Galvicon : un produit discontinué depuis 30 ans
Dans plusieurs devis, appels d’offres et discussions de chantier, le terme « Galvicon » continue d’être utilisé comme solution de retouche pour l’acier galvanisé. Le
La corrosion galvanique est un phénomène qui se produit lorsque deux métaux différents sont en contact électrique direct et sont également exposés à un électrolyte, comme de l’eau ou une solution saline. Le métal le plus réactif (ou le moins noble) de la paire devient l’anode et commence à se corroder, tandis que le métal plus noble devient la cathode et ne se corrode pas.
Lorsque ces deux métaux sont en contact, il se produit une réaction électrochimique qui entraîne une migration d’électrons de l’anode (le métal plus réactif) vers la cathode (le métal plus noble). Ce flux d’électrons résulte en une corrosion accélérée de l’anode, alors que la cathode reste intacte.
La série galvanique permet de prédire quel métal sera l’anode et lequel sera la cathode dans une paire de métaux donnée. Plus la différence entre les deux métaux dans la série galvanique est grande, plus la corrosion galvanique sera rapide. Par exemple, si du zinc et de l’acier inoxydable sont en contact, le zinc sera l’anode et se corrodera plus rapidement que l’acier inoxydable, qui sera la cathode.
|
Platine |
|
Or |
|
Argent |
|
Acier inoxydable (Stainless) |
|
Cuivre |
|
Fonte |
|
Acier |
|
Aluminium |
|
Zinc (acier galvanisé) |
|
Magnésium |
Il existe plusieurs moyens pour éviter la corrosion galvanique : 1. Sélectionner des métaux ayant une différence de potentiel électrique minimale.
Le tableau ci-dessous indique les combinaisons de métaux acceptables et celles à éviter afin de minimiser le risque de corrosion galvanique en fonction des choix de matériaux effectués.
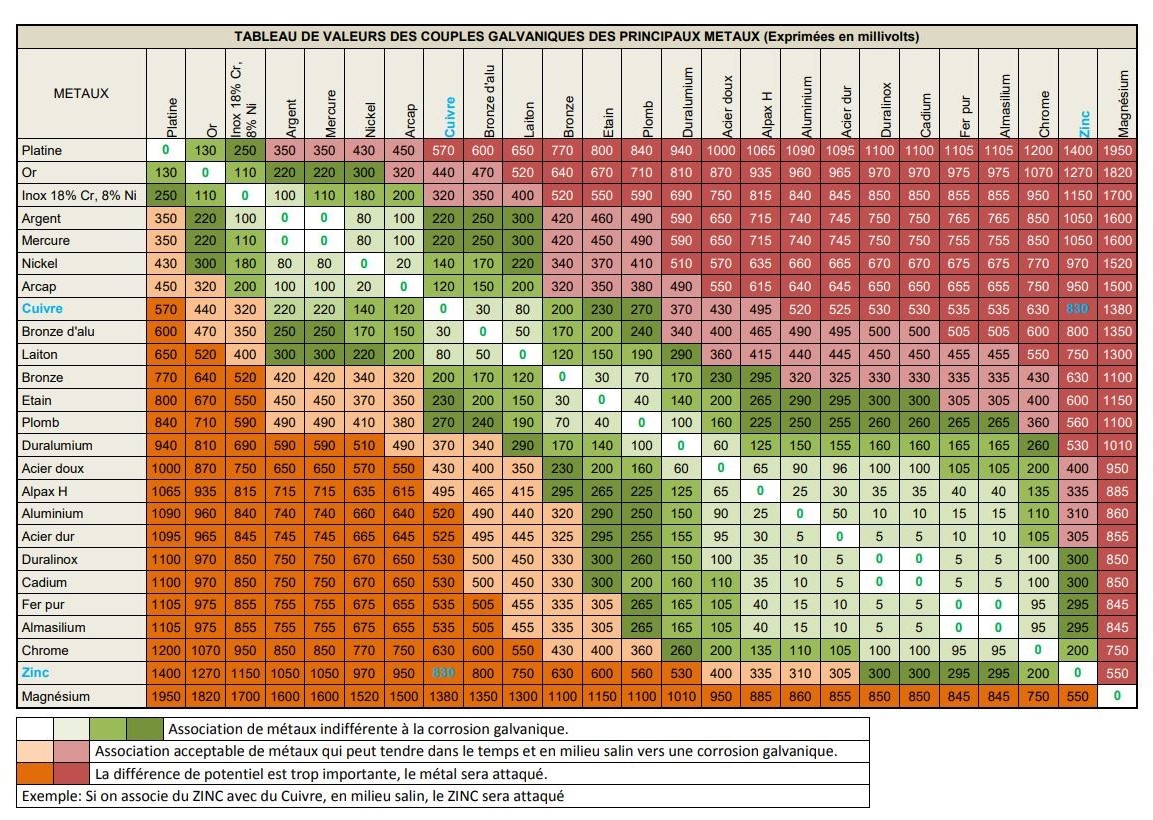
2. Utiliser des joints en caoutchouc ou en plastique : en ajoutant des joints en caoutchouc ou en plastique entre les métaux, on peut éviter le contact direct et ainsi éviter la corrosion galvanique.
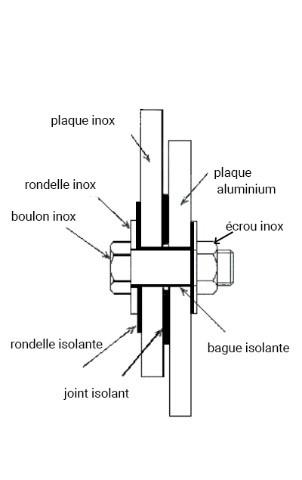
3. Utiliser les enduits Rust-Anode : l’utilisation des enduits Rust-Anode constitue une solution efficace pour protéger les structures en acier contre la corrosion. Grâce à notre technologie de zinc, nos enduits offrent une protection galvanique en se sacrifiant pour préserver l’acier qui elle restera cathodique. En appliquant une couche de notre produit sur les métaux dissimilaires en contact, nos enduits assumeront la charge anodique de l’assemblage, prévenant ainsi la corrosion galvanique des deux métaux en contact.
4. Utiliser des anodes sacrificielles : en ajoutant des anodes sacrificielles en métal moins noble que les autres métaux en contact, on peut réduire la corrosion galvanique en faisant en sorte que l’anode sacrifiée se corrode plutôt que les autres métaux. Ces anodes sacrifient leur propre durabilité pour protéger le métal plus noble. Par exemple, des anodes sacrificielles en zinc, en aluminium ou en magnésium ont été utilisées pour protéger l’acier de la corrosion dans l’eau de mer.

Il est essentiel de souligner que la prévention de la corrosion galvanique commence dès la conception d’un projet, en prenant en considération le choix des matériaux afin d’éviter tout contact entre les métaux susceptibles de causer cette corrosion. Les enduits Rust-Anode constituent une solution efficace pour la protection de l’acier grâce à leur mécanisme de protection cathodique, garantissant ainsi la durabilité des structures traitées.
Contactez-nous pour en apprendre davantage. 1-888-743-2046Dans plusieurs devis, appels d’offres et discussions de chantier, le terme « Galvicon » continue d’être utilisé comme solution de retouche pour l’acier galvanisé. Le
Galvatech 2000 est à la recherche d’un·e Directeur·trice du développement des affaires pour jouer un rôle clé dans sa croissance, au Québec et à l’international.
Préparer, appliquer et contrôler avec précision Dans l’industrie des revêtements, un devis clair est bien plus qu’un simple outil pour établir des coûts. C’est une